近期,我校hjc356黄金城首页线路周楠迪教授团队在NO检测方面取得重要进展,研究成果“Ratiometric fluorescent biosensor for detection and real-time imaging of nitric oxide in mitochondria of living cells”正式发表于Biosensors and Bioelectronics (IF =/info/1021/ /12.6) (https://doi.org/10.1016/j.bios.2024.116000)。
一氧化氮(NO)是一种重要的气体信使分子,通过内源性细胞中的L-精氨酸在一氧化氮合酶(NOS)的作用下产生。NO在各种生化过程中起着关键作用,如血管扩张、血压调节、神经保护和抑制炎症反应等。而线粒体是哺乳动物细胞中产生一氧化氮的主要亚细胞器。最近的研究表明,一氧化氮对线粒体功能具有精细调节作用,例如调节线粒体呼吸链、调节线粒体膜电位和调节线粒体氧化应激反应。然而,由于一氧化氮浓度低、半衰期短且容易被氧化,研究其在生物系统中的各种功能面临许多挑战和障碍。因此,迫切需要开发敏感准确的线粒体内一氧化氮检测方法,以更好地阐明其在生理和病理过程中的作用。
周楠迪教授团队开发了一种基于金属荧光增强效应(MEF)的比例荧光生物传感器Mito-GNP-pNO520,用于活细胞线粒体NO的检测和实时成像。首先设计并合成了一个荧光峰位于520 nm处的NO响应探针(pNO520)。随后,定向制备了与pNO520光谱重叠明显的纳米金球(GNP)。通过引入不同碱基对数目(bp)的双链DNA (dsDNA)来调整GNP与pNO520之间的距离。最后,在GNP表面修饰线粒体靶向肽(MLS),使其特异性靶向线粒体。在没有NO的情况下,由于邻苯二胺和萘酰亚胺之间的光诱导电子转移效应(PET), Mito-GNPpNO520显示出极弱的荧光。然而,NO在O2存在下与Mito-GNP-pNO520反应形成苯并三唑衍生物(NO520),通过抑制PET效应表现出荧光开启。无论是否存在NO, Mito-GNP-pNO520中Cy5的荧光强度保持不变。因此,可以根据NO520与Cy5的荧光强度比对NO进行定量检测和荧光成像。该传感器在1 ~ 90 nM的浓度区间内对NO浓度表现出良好的线性响应,检测限低至0.25 nM。本研究在线粒体NO的检测和实时成像方面具有广阔的前景,且具有较低的检测限以及较高的稳定性和特异性,为探索亚细胞水平NO相关的生理病理信息提供了有力的工具。
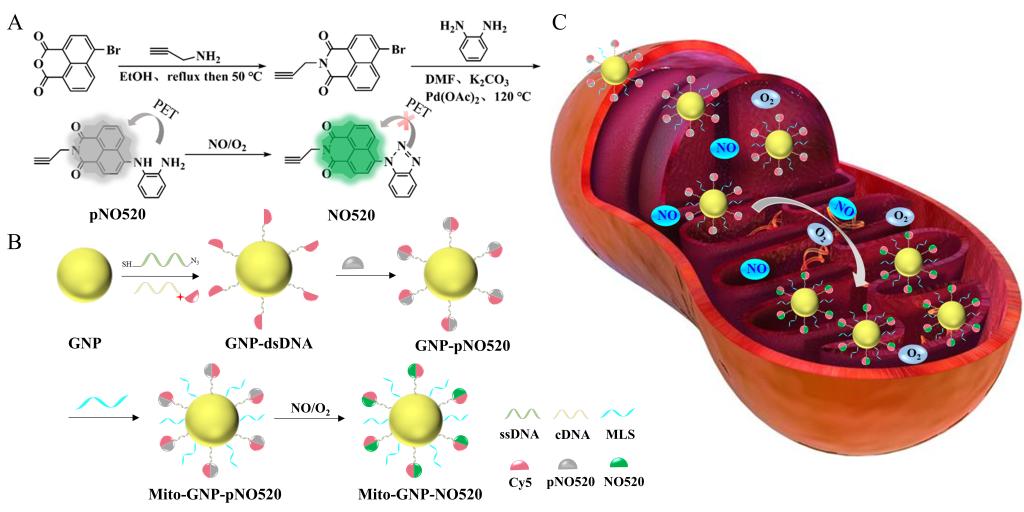
图形摘要
王晓丽副教授为论文的通讯作者,我校2021级硕士生刘浩为第一作者。上述研究得到了国家自然科学基金(32371430、62301234)和糖化学与生物技术教育部重点实验室开放课题(KLCCB-KF202201)等资助。
近年来周楠迪教授团队研究方向包括核酸适配体的筛选优化和应用、分子诊断技术、新型纳米生物传感器的研制、智能纳米器件的构建和应用、POCT产品研制、食品安全检测、发酵过程中代谢物监测等方面。相关研究成果已发表在Analytical Chemistry (2023)、Biosensors and Bioelectronics (2022、2022、2021)、Food Chemistry (2022)、Talanta (2022)、Sensors and Actuators B: Chemical (2021)、ACS Applied Materials & Interfaces (2021) 等本领域权威期刊。
