近日,我校糖化学与生物技术教育部重点实验室、未来食品科学中心康振教授课题组在3′-磷酸腺苷-5′-磷酸硫酸(PAPS)生物合成领域取得新突破,研究成果“Closed-Loop System Driven by ADP Phosphorylation from Pyrophosphate Affords Equimolar Transformation of ATP to3′-Phosphoadenosine-5′-phosphosulfate”以封面形式发表了在ACS Catalysis(https://pubs.acs.org/doi/10.1021/acscatal.1c02004),2020级博士生胥睿睿和副研究员王阳为该论文共同第一作者,康振教授为通讯作者。
PAPS是生物体内所有生物磺酸化反应的通用磺酸基团供体,其生物催化合成一直是一个难题,困扰着含磺酸基团化合物如肝素和硫酸软骨素的合成研究。现有PAPS的酶法合成面临着天然转化率低(2 mol ATP只能合成1 mol PAPS,50%)和高成本的障碍。针对现有问题,研究人员设计创建了一条理论转化率为100%的PAPS合成路线。
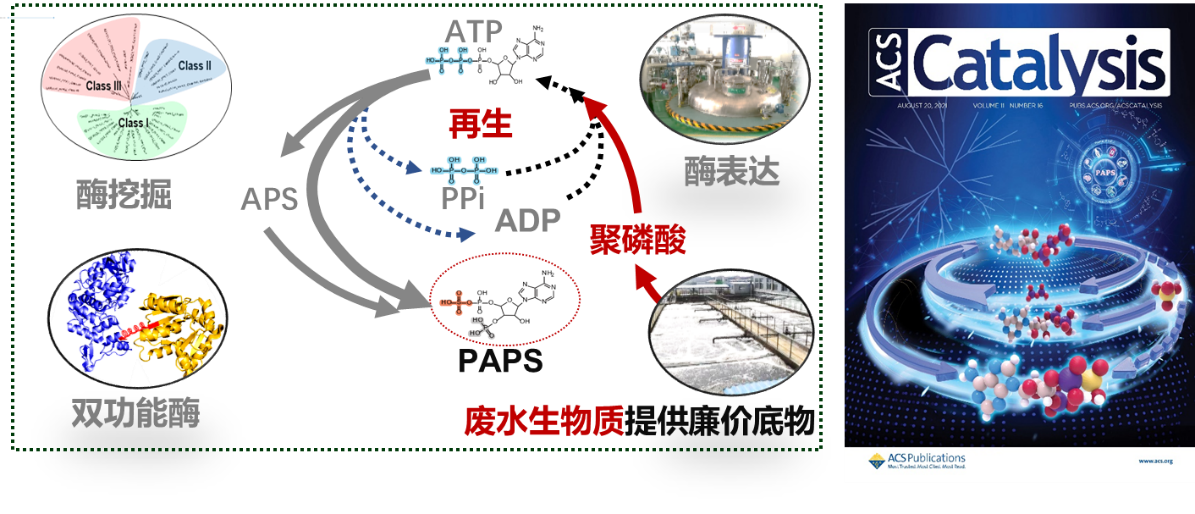
通过融合来自不同物种的腺苷5′-三磷酸硫酰化酶和腺苷5′-磷酸硫酸激酶,人工创造了一种具有活性的双功能酶来直接将ATP转化为PAPS。为了最大限度地将ATP转化为PAPS,通过系统挖掘成功获得以廉价聚磷酸为高能磷酸供体的聚磷酸激酶。在此基础上,设计并构建了一个依赖于聚磷酸盐的ATP再生系统。研究人员进一步发现焦磷酸PPi可以作为磷酸供体,驱动ADP实现ATP再生。最终,成功创建了一条闭环ATP再生途径,实现了理论转化率由50%突破为100%。本研究开发的低成本高效酶法合成PAPS路线对推动磺酸基团化合物的生物合成具有重要意义。
上述研究得到了国家重研发计划(2021YFC2100800)、江苏省杰出青年科学基金(BK20200025)、国家自然科学基金(32000058、31970085)、关键技术资助江苏省研发计划(BE2019630),国家轻工技术与工程一流学科(LITE2018-16)的资助。