近期,我校hjc356黄金城首页线路刘立明教授团队在脂肪族氨基酸远程C(sp3)-H键羟基化区域选择性调控方面取得重要进展,研究成果“Rational Design of the Spatial Effect in a Fe(II)/α-Ketoglutarate Dependent Dioxygenase Reverses the Regioselectivity of C(sp3)-H Bond Hydroxylation in Aliphatic Amino Acids”正式发表于Angewandte Chemie International Edition (IF =/info/1021/ /16.1) (https://doi.org/10.1002/anie.202406060)。
脂肪族羟基氨基酸是一类广泛用于制药、食品和生物基材料的多功能非天然氨基酸。目前其需求量高,合成方法有限,迫切需要开发高效且绿色的脂肪族羟基氨基酸合成方法。直接羟基化脂肪族氨基酸侧链的C(sp3)-H键具有高原子经济性和步骤经济性。然而,该方法存在两个主要挑战:(i) 主链中高活性的氨基和羧基以及侧链中多个相似键强度的C(sp3)-H键影响特定位点的羟基化反应;(ii) 在竞争性近端C(sp3)-H键存在的情况下,难以实现远程C(sp3)-H键羟基化反应。Fe(II)/αKG依赖型双加氧酶能够催化各种脂肪族氨基酸侧链C(sp3)-H键羟基化反应,被视为不对称合成羟基氨基酸的重要催化剂,但仍缺乏对脂肪族氨基酸远程C(sp3)-H键羟基化反应的生物催化剂。
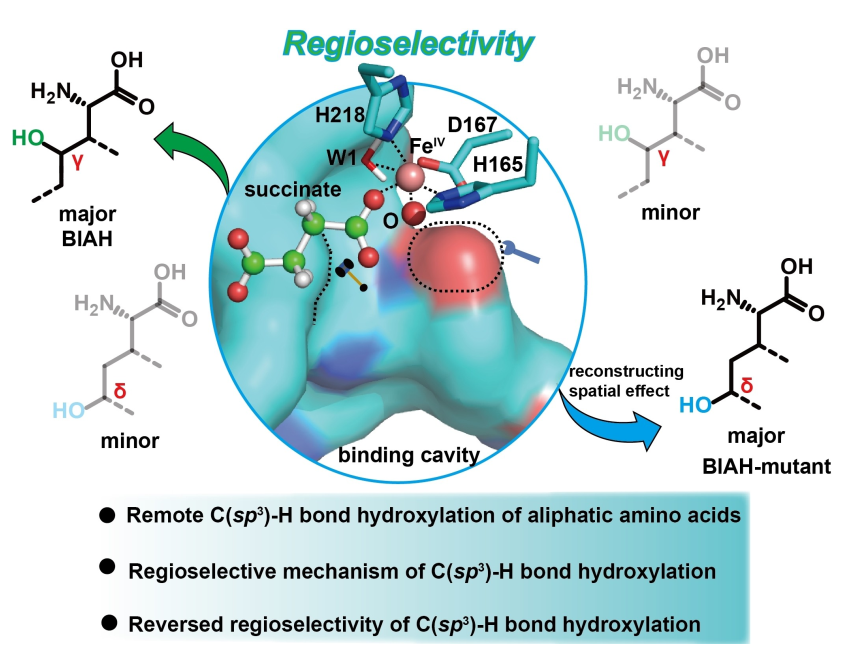
刘立明教授团队针对脂肪族氨基酸远程C(sp3)-H键羟基化的合成挑战,通过理性设计Fe(II)/αKG依赖型双加氧酶的空间效应实现远程羟基氨基酸的生物合成。首先,筛选出来自芽孢杆菌的Fe(II)/αKG依赖型双加氧酶BlAH,其对多种脂肪族氨基酸底物具有羟基化活性。随后,采用LC-MS和NMR对产物结构的鉴定发现BlAH对多种氨基酸底物具有γ位C(sp3)-H键羟化活性,其中对L-正亮氨酸和L-高亮氨酸具有γ和δ位C(sp3)-H键混杂的羟基化活性。为实现专一性氨基酸远程δ位C(sp3)-H键羟基化功能,本研究拟从酶的区域选择性机制入手进行研究。DFT计算表明在没有酶骨架的参与下,氨基酸远程γ位C(sp3)-H键发生羟基化反应的能垒远低于δ位,表明在羟基化反应中更易生成γ位羟基化产物。然而,计算预测与实验观测到δ位羟化产物相矛盾,因此我们推测酶骨架与底物的结合能够逆转底物固有的反应性。随后,分析晶体结构和MD模拟发现:(1)酶与氨基酸底物的主链以一种固定的结合模式结合;(2)氨基酸底物侧链的结合具有多样性;(3)酶与L-正亮氨酸结合时对其δ位过渡态结构具有更高的稳定性(-35.5 ± 1.7 kcal mol-1 (δ位过渡态结合能) vs -30.6 ± 1.2 kcal mol-1 (γ位过渡态结合能)),进一步证明酶骨架能够影响底物侧链的结合姿势,进而影响酶的区域选择性。对结构分析发现,可能是由于L237和Y87残基的空间效应影响了底物的结合,使酶具有混杂的羟化功能。通过上述研究表明,BlAH侧链结合腔的空间效应影响了氨基酸底物侧链结合姿势导致了酶的区域选择性。因此,设想通过设计侧链结合腔的空间效应来稳定δ位C(sp3)-H键的过渡态结构进而实现氨基酸远程δ位C(sp3)-H键的羟基化反应。作为概念验证,对底物L-正亮氨酸和L-高亮氨酸进行了区域选择性调控,成功实现L-正亮氨酸区域选择性从1:11.2(δ:γ)逆转为3.5:1,对L-高亮氨酸的区域选择性从1:12逆转为>99:1,并结合MD模拟分析了其区域选择性逆转的分子机制。
hjc356黄金城首页线路2021级博士研究生郑晨妮为论文第一作者,刘立明教授为论文的通讯作者。上述研究工作得到了国家重点研发计划(2021YFC2100100)、国家轻工业技术与工程一流学科项目(QGJC20230101)、江南大学食品科学与资源挖掘全国重点实验室研究项目(SKLF-ZZB-202303)等资助。
近年来刘立明教授领衔的江苏省科技创新团队以合成生物学科学理论为指导,在系统开展高效合成高值化合物细胞工厂构建及酶工程方面取得丰硕成果,相关研究成果已发表在Nature Communications (2024)、Angewandte Chemie International Edition (2024)、Chemical Engineering Journal (2024)、ACS Sustainable Chemistry & Engineering (2024)、Metabolic Engineering (2024)等本领域权威期刊。
